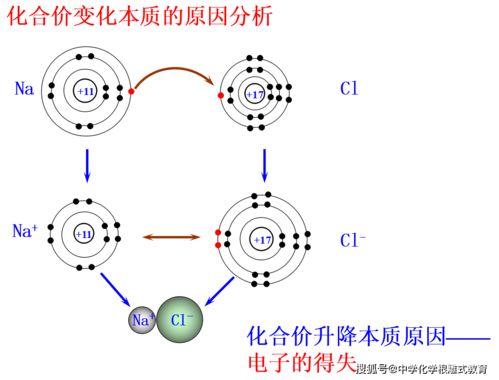
氧化还原反应的实质是电子的转移,这种电子的转移使得原子核的氧化态和还原态发生变化,从而产生了化学反应。
2. 氧化还原反应的定义
氧化还原反应是一种化学反应,其中原子失去或获得电子,以形成新的化合物。这种反应可以通过电子的转移来实现,其中氧化剂接受电子,而还原剂则失去电子。
3. 氧化还原反应的实质
氧化还原反应的实质是电子的转移。在氧化还原反应中,氧化剂接受电子,而还原剂则失去电子。这种电子的转移使得原子核的氧化态和还原态发生变化,从而产生了化学反应。
4. 氧化还原反应的应用
氧化还原反应在许多领域都有广泛的应用,例如化学工业、生物学和医学。例如,在化学工业中,氧化还原反应可以用于金属的冶炼和合成药物。在生物学中,氧化还原反应可以用于细胞呼吸和光合作用。在医学中,氧化还原反应可以用于治疗癌症和心血管疾病。
5. 氧化还原反应的分类
氧化还原反应可以根据电子的转移方式进行分类,包括电子转移反应、电子对转移反应和氧化还原合成反应。
6. 氧化还原反应的电子转移方式
氧化还原反应的电子转移方式包括电子的转移、电子对转移和氧化还原合成反应。其中,电子转移是最常见的氧化还原反应方式,它指的是原子失去或获得一个或多个电子。
7. 氧化还原反应的电子对转移
电子对转移是另一种氧化还原反应方式,它指的是两个原子之间共享电子对。这种反应通常发生在具有共价键的化合物中,例如共轭酸和共轭醇。
8. 氧化还原反应的氧化态和还原态
氧化还原反应中,氧化态是指原子核的电子数,而还原态则是指原子核的电子数减去一个或多个电子。氧化态和还原态的差值称为氧化还原电荷。
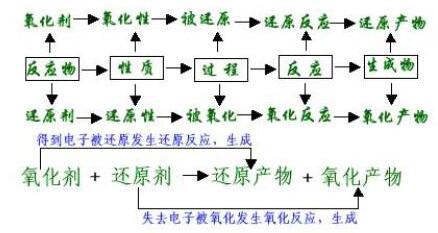
9. 氧化还原反应的氧化剂和还原剂
氧化剂是指能够接受电子的物质,而还原剂则是指能够捐赠电子的物质。
10. 氧化还原反应的化学方程式
氧化还原反应的化学方程式可以用来描述化学反应中电子的转移。例如,下面的化学方程式表示了氢气在氧气中燃烧的反应:
2H2 + O2 → 2H2O
在这个方程式中,氢气是还原剂,而氧气是氧化剂。
本文内容来自互联网,若需转载请注明:https://bk.66688891.com/13/168163.html